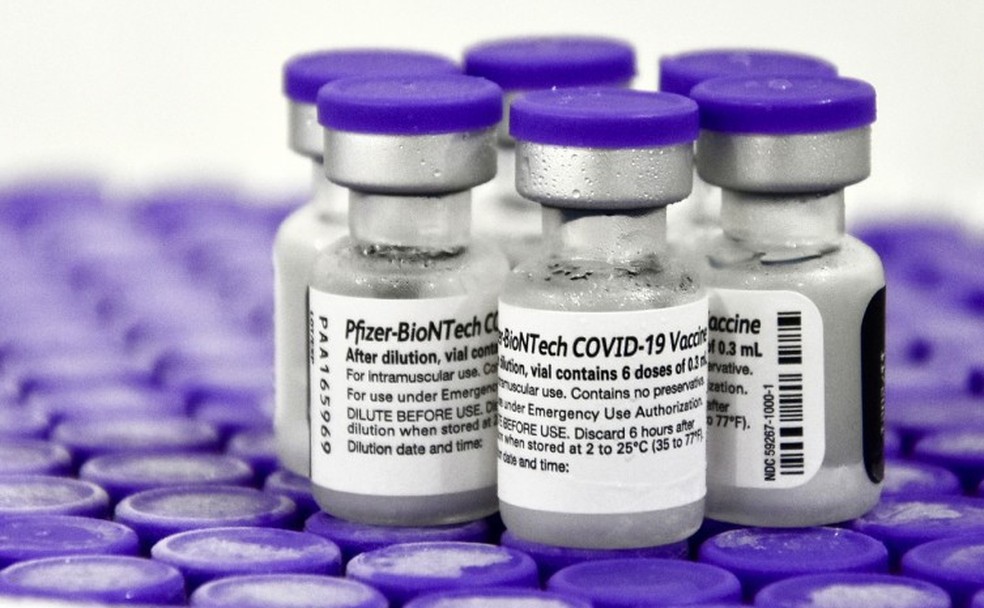
A Agência Nacional de Vigilância Sanitária (Anvisa) vai autorizar a aplicação da vacina da Pfizer, contra a covid-19, em crianças de 5 a 11 anos. A área técnica do órgão se reúne publicamente nesta quinta-feira (16), após terminar a análise do pedido da fabricante, para apresentar relatório sobre a imunização desta faixa etária. Com a liberação, a decisão da Anvisa precisará ser publicada no Diário Oficial da União para passar a valer. Enquanto isso, Doria protocolou na tarde desta quarta-feira (15) pedido de autorização para aplicar a vacina paulista em crianças a partir de três anos até adolescentes de 17 anos. Governador de SP diz que a mesma vacina está sendo utilizada nessa faixa etária em diversos países e que pais brasileiros aguardam com ansiedade avacinação dos filhos.

A Pfizer já tem o registro definitivo da vacina no Brasil. Com a autorização da área técnica da Anvisa, a bula do imunizante será alterada para inclusão das crianças de 5 a 11 anos. O tema não necessitará de aprovação da diretoria colegiada. O início da vacinação depende do Ministério ou das secretarias de Saúde, e cronogramas ainda não foram informados.
Casos graves da covid-19 entre crianças são menos frequentes, mas o imunizante ajuda a dar proteção mais ampla a essa faixa etária, além de reduzir o risco de que elas se tornem transmissores do vírus para parentes e professores. A vacina da Pfizer entre os mais novos passou por testes de segurança e eficiência.

A Anvisa recebeu a notificação da agência americana em 12 de novembro. Na ocasião, o laboratório submeteu ao órgão dados e os estudos de segurança para embasar o pedido de vacinação de crianças. Além do corpo técnico da Agência, representantes de sociedades médicas brasileiras também participaram da análise do pedido da fabricante.

Ao pedir autorização, a Pfizer afirmou que a dosagem da vacina para a faixa etária seria ajustada e menor do que aquela aplicada em maiores de 12 anos. A proposta é ter frascos diferentes, com dosagem específica para cada grupo (maiores ou menores de 12 anos). Segundo a empresa, os frascos serão diferenciados pela cor.
O Ministério da Saúde começou a se preparar para a vacinação de crianças em novembro, antes da autorização da Anvisa. A pasta decidiu se antecipar e negociou com a Pfizer 40 milhões de doses para imunizar a faixa etária de 5 a 11 anos. A entrega dos imunizantes estava condicionada ao aval do órgão.
A vacinação de crianças enfrenta resistência do presidente Jair Bolsonaro e de apoiadores da ala ideológica. No fim de outubro, antes de a Pfizer pedir a inclusão das crianças na bula do imunizante, diretores da Anvisa foram ameaçados de morte por e-mail por um homem do Paraná. A mensagem foi repassada a diferentes órgãos de investigação.
A vacina da Pfizer está registrada no País desde 23 de fevereiro deste ano. Inicialmente, o imunizante foi autorizado para pessoas com mais de 16 anos. Em 11 de junho, a Anvisa liberou a inclusão da faixa etária de 12 a 15 anos.
Em agosto, a agência negou autorização para a aplicação do imunizante Coronavac contra a covid-19 em crianças e adolescentes de 3 a 17 anos. O pedido havia sido feito pelo Instituto Butantan, produtor da vacina no Brasil. A decisão apontava que os dados apresentados pelo instituto não eram suficientes para comprovar a segurança da vacina no grupo pediátrico. O instituto paulista já fez novo pedido.
Produto já foi liberado nos EUA
A vacina da Pfizer já está liberada nos Estados Unidos para crianças de 5 a 11 anos desde o dia 2 de novembro. Lá, a vacina é aplicada em duas doses com três semanas de intervalo. A dose foi ajustada para um terço por injeção em comparação com a aplicada em adultos e adolescentes. A aprovação da Agência de Medicamentos dos Estados Unidos (FDA), dizem especialistas, pesa favoravelmente para que o mesmo acontecesse no Brasil.
Pedido do Butantan
O Governador João Doria confirmou na tarde desta quarta-feira (15), em Brasília, que o Instituto Butantan fez um novo pedido oficial à Anvisa (Agência Nacional de Vigilância Sanitária) para uso da Coronavac na vacinação de crianças e jovens com idade entre 3 e 17 anos. A primeira solicitação já havia sido formalizada em agosto.
“Nos últimos meses o Governo de São Paulo e o Instituto Butantan, maior fabricante de vacinas do hemisfério sul, têm solicitado que a Anvisa avalie e autorize a vacinação de crianças e jovens. Não há razão para uma protelação tão longa”, afirmou Doria. “Nós confiamos na Anvisa, mas é hora de se tomar uma decisão antes das férias de Natal e Ano Novo. Lembrando que países vizinhos já estão vacinando nesta faixa”, acrescentou.
Há uma semana, Doria anunciou a reserva de 12 milhões de doses da Coronavac para a vacinação de crianças. A meta em São Paulo é iniciar a aplicação da Coronavac em menores de 18 anos imediatamente após um eventual comunicado positivo da Anvisa em relação ao novo pedido do Butantan. Até agora, apenas a vacina da Pfizer é usada na vacinação de jovens a partir de 12 anos.
Vacinômetro
Atualmente, São Paulo é líder da vacinação contra o coronavírus em termos quantitativos e proporcionais no Brasil. O estado também ocuparia o terceiro lugar entre nações que mais vacinam e contam com mais de 40 milhões de habitantes, segundo o portal Our World In Data, ligado à Universidade de Oxford.
De acordo com o Vacinômetro (https://vacinaja.sp.gov.br/), mais de 81,8 milhões de doses já foram aplicadas em São Paulo até o final da tarde desta quarta. Mais de 95% da população paulista com mais de 18 anos está com esquema vacinal completo. Incluindo jovens de 12 a 17 anos na campanha, a imunização completa em São Paulo já protege mais de 78% de toda a população.